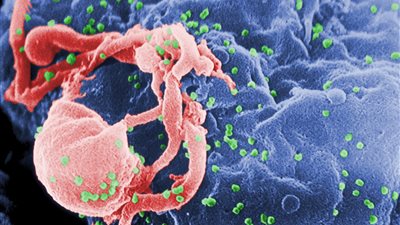
طريقة جديدة لتطوير أدوية فيروس نقص المناعة البشرية
نجح فريق من الباحثين في جامعة ميشيجان في تعديل مركب كيميائي طبيعي في المختبر، ما أدى إلى إنتاج مركبات رصاص متقدمة ذات نشاط مضاد لفيروس نقص المناعة البشرية.
وفقا لموقع ميديكال إكسبريس، تقدم نتائجهم، المنشورة في مجلة الكيمياء الطبية، طريقًا جديدًا للمضي قدمًا في تطوير الأدوية التي يمكن أن تساعد في علاج فيروس نقص المناعة البشرية.
وبالرغم من توفر علاجات فعالة لإدارة فيروس نقص المناعة البشرية، فإن العلاج ظل بعيد المنال بسبب قدرة الفيروس على الاختباء من الجهاز المناعي، حيث يظل كامنًا في خزانات الخلايا المصابة.
وقالت كاثلين كولينز، أستاذة علم الأحياء الدقيقة والمناعة في كلية الطب بجامعة ميريلاند: «في حالة معظم الفيروسات، عندما يصاب الناس بالعدوى، فإنهم يمرضون لفترة من الوقت، ثم يبدأ الجهاز المناعي في التخلص من الفيروس، ولكن في حالة فيروس نقص المناعة البشرية، بمجرد إصابة المريض، سيستمر هذا الفيروس طوال حياته، مما يعني أنه يجب أن يظل تحت العلاج إلى أجل غير مسمى».
تخفي فيروس نقص المناعة البشرية
أحد مفاتيح قدرة فيروس نقص المناعة البشرية على البقاء مخفيًا في خلايا المرضى هو البروتين الذي يصنعه الفيروس ويسمى Nef.
يقوم هذا البروتين بإيقاف النظام الذي تستخدمه الخلية عادة لتنبيه الجهاز المناعي إلى العدوى، وبالتالي يمنع الخلايا المناعية من التعرف على الفيروس والقضاء عليه.
قامت كولينز ومختبرها بدراسة هذا البروتين لأكثر من 15 عامًا، وبحثوا في كيفية عمله وكيف يمكن تعطيله.
اكتشفت هي وديفيد شيرمان، الأستاذ في معهد علوم الحياة بجامعة UM، سابقًا أن مادة كيميائية موجودة في الطبيعة يمكن أن تمنع فيروس نقص المناعة البشرية Nef، مما يسمح لجهاز المناعة بالعثور على الخلايا المصابة بالفيروس والقضاء عليها: مركب يسمى كونكاناميسين A (CMA)، والذي يتم إنتاجه بواسطة الكائنات الحية الدقيقة المشتقة من التربة.
ومع ذلك، في شكله الطبيعي، يقدم CMA العديد من التحديات باعتباره علاجًا محتملًا.
كان التحدي الأول الذي كان على الفريق التغلب عليه هو العرض، في حين أن CMA مركب طبيعي، فإن البكتيريا الأصلية التي تنتجه تفعل ذلك بكميات صغيرة جدًا بحيث لا تكون مفيدة للاختبار والتعديل في المختبر.
التحدي الرئيسي الآخر الذي يواجه تطوير CMA كدواء مضاد لفيروس نقص المناعة البشرية هو أن Nef ليس الهدف الأساسي لـ CMA.
وقال شيرمان، وهو أيضًا أستاذ في كلية الصيدلة وكلية الطب والكلية بجامعة UM: «إن الوظيفة الرئيسية لـ CMA في الخلايا البشرية هي تثبيط إنزيم يسمى V-ATPase، والذي لا نريد على الإطلاق حظره في هذه الحالة، لذا، كنا بحاجة إلى إيجاد طريقة لتعديل نشاط CMA، وتوسيع فجوة الجرعة الفعالة بين الوقت الذي يبدأ فيه في تثبيط الهدف الذي نهدف إليه -HIV Nef- دون التأثير على V-ATPase، هدفه الخلوي النموذجي».
وبفضل هذا البحث الأخير، تغلب الفريق على هذين التحديين، وباستخدام الهندسة الحيوية، تمكن فريق شيرمان من تطوير سلالة بكتيرية زادت إنتاج CMA بمقدار 2000 مرة.
بعد ذلك، ابتكر الكيميائيون الاصطناعيون في المختبر أكثر من 70 نوعًا جديدًا من المركب، وقاموا باستبدال مجموعات كيميائية مختلفة لاختبار فعاليتها ضد فيروس نقص المناعة البشرية Nef.
أجرى فريق مختبر كولينز المركبات الجديدة من خلال مجموعة من الاختبارات لقياس سميتها للخلايا، وكذلك كيفية تأثيرها على أنشطة كل من فيروس نقص المناعة البشرية Nef وV-ATPase.
وقال كولينز، وهو أيضا أستاذ الطب الباطني في كلية الطب: «بالرغم من أننا نعلم أن CMA نشط للغاية ضد بروتين فيروس نقص المناعة البشرية Nef، إلا أن جميع الأدوية لها آثار جانبية، ولذلك أردنا التأكد من أننا بذلنا كل ما في وسعنا لتقليل الآثار الجانبية للدواء قبل أن نفكر في تطبيقه على الحيوان أو الإنسان».
يمتلك الفريق الآن العديد من نظائر CMA التي تظهر فعالية عالية في منع فيروس نقص المناعة البشرية Nef عند مستويات جرعات منخفضة جدًا دون مقاطعة التأثيرات غير المستهدفة أو التسبب في سمية الخلايا البشرية.
ومع ذلك، يحذرون من أنه لا تزال هناك عدة خطوات مهمة قبل أن تصبح المركبات جاهزة لمزيد من الاختبارات في بيئة سريرية.