اكتشاف جديد بخصوص سرطان الخلايا الحرشفية في الجلد
تمكن علماء من تحديد الآليات الأيضية الرئيسية التي تستخدمها سرطانات الخلايا الحرشفية في الجلد لمقاومة العلاج، مما يوفر رؤى جديدة حول كيفية إيقاف نمو السرطان.
وتسلط النتائج التي نشرت في مجلة Science Advances الضوء على الحاجة إلى علاجات مركبة تستهدف مسارات أيضية متعددة في وقت واحد.
وقد يؤدي هذا النهج إلى علاجات أكثر فعالية ليس فقط لسرطان الخلايا الحرشفية في الجلد، والذي يتكون في الخلايا الموجودة على سطح الجلد، ولكن أيضًا للعديد من أنواع السرطان الأخرى التي تشترك في السمات الأيضية المماثلة، وفق ما نشره موقع ميديكال إكسبريس.
أجرى البحث المؤلف الرئيسي ويليام لوري، أستاذ علم الأحياء الجزيئي والخلوي والتنموي في جامعة كاليفورنيا في لوس أنجلوس.
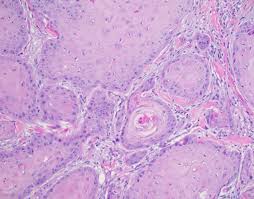
تأثير واربورج
في عام 2019، قلب لوري وزملاؤه عقيدة أساسية في نظرية التمثيل الغذائي للسرطان المعروفة باسم تأثير واربورج، والتي تنص على أن خلايا السرطان تعتمد في المقام الأول على الجلوكوز للحصول على الطاقة.
وبدلًا من ذلك، وجدوا أن خلايا سرطان الخلايا الحرشفية في الجلد مرنة من الناحية الأيضية: عندما لا يتوفر الجلوكوز، يمكنها التحول إلى استخلاص الطاقة من حمض الجلوتامين الأميني.
وقال لوري، المدير المساعد للتعليم ونقل التكنولوجيا في مركز أبحاث الخلايا الجذعية بجامعة كاليفورنيا في لوس أنجلوس: "تشير بياناتنا إلى أن السبب وراء فشل الجهود السريرية السابقة لاستهداف عملية التمثيل الغذائي للسرطان هو أنها ركزت على مسار واحد فقط في كل مرة".
وأضاف: "يوجد في الكائن الحي العديد من العناصر الغذائية المتاحة التي يمكن للأورام استخدامها لتغذية نموها، مما يجعل التدخلات ذات المسار الواحد غير كافية."
وبناءً على هذا العمل، قام كارلوس جالفان، وهو طالب دراسات عليا في مختبر لوري، والمؤلف الأول للدراسة الجديدة، بالتحقيق في مدى هذه المرونة الأيضية وما إذا كان من الممكن الحد منها.
وباستخدام نماذج الفئران، نجح في منع المسار الذي يستخدمه الجلوتامين لتغذية الخلايا في الخلايا الجذعية لبصيلات الشعر ـ وهو نوع معروف من الخلايا المنشأ لسرطان الخلايا الحرشفية في الجلد ـ ولاحظ تأثيره على تكوين الأورام ونموها.
وكما حدث في التجارب السابقة، تحولت الأورام ببساطة إلى مصدر غذائي آخر.
قال جالفان، الذي يشارك أيضًا في برنامج تدريب مركز أبحاث الخلايا الجذعية بجامعة كاليفورنيا في لوس أنجلوس: "إن الأمر يشبه لعبة ضرب الخلد، فعندما يتم حجب مسار أيضي واحد، تصبح الخلايا السرطانية مرنة بما يكفي للعثور على عنصر غذائي آخر لتغذية نموها".
وبعد ذلك، حاول الباحثون ما أطلقوا عليه أسلوب "المطرقة المزدوجة": حجب المسارات الوراثية لكل من الجلوكوز والجلوتامين عن طريق حذف الناقل الذي يسمح بامتصاص الإنزيمات المعنية، وكانت استراتيجية الهدف المزدوج هذه كافية لمنع نمو السرطان في نماذج الفئران.
وسعى جالفان أيضًا إلى تحديد الآليات التي مكنت الخلايا السرطانية من إعادة برمجة برامجها الأيضية لمواصلة النمو عندما تم حظر أحد مسارات المغذيات.
ومن المثير للاهتمام أنه وجد أن المرونة الأيضية لم تكن مدفوعة باستجابة نسخية، كما كان يُشتبه في البداية، ولكن من خلال إعادة توزيع سريع لبروتينات النقل إلى غشاء الخلية، مما يسمح للخلايا بامتصاص العناصر الغذائية البديلة.
ويعمل فريق البحث على تكرار النتائج الجينية التي توصلوا إليها باستخدام مثبطات دوائية لاستهداف الإنزيمات المحددة التي تشارك في هذه العمليات الأيضية. ولإيصال هذه الاستراتيجية العلاجية للمرضى، يركز الفريق على تحديد واختبار التركيبة الصحيحة من الأدوية التي يمكنها تحقيق نفس التأثيرات التي لوحظت مع التلاعب الجيني.
وإضافة إلى ذلك، يبدي الباحثون اهتمامًا بتطوير علاج موضعي يمكن تطبيقه مباشرة على الجلد.
ويقدم هذا النهج ميزة فريدة: استهداف موقع الورم على وجه التحديد، مما يقلل من الآثار الجانبية التي غالبًا ما نراها مع العلاجات الفموية.
قال جالفان: "إن إحدى مزايا علاج سرطان الجلد هي إمكانية الوصول إلى الورم، إن تطبيق العلاج موضعيًا، باستخدام هلام أو غسول، قد يكون أكثر فعالية وأمانًا من العلاجات الجهازية. لكننا لا نزال نواجه تحديات، مثل ضمان قدرة الدواء على اختراق حاجز الجلد والحفاظ على فعاليته بمرور الوقت".
وبما أن أنواعًا أخرى من السرطان تستخدم أيضًا الجلوكوز والجلوتامين لتغذية نموها، فإن تداعيات الدراسة تمتد إلى ما هو أبعد من سرطان الخلايا الحرشفية في الجلد.
ويعمل الباحثون حاليًا على تطبيق هذه الاستراتيجية على أنواع أخرى من السرطان، مثل الورم الميلانيني.
ويقوم الباحثون أيضًا باستكشاف البروتين والتنظيم ما بعد النسخي الذي يتيح المرونة الأيضية.