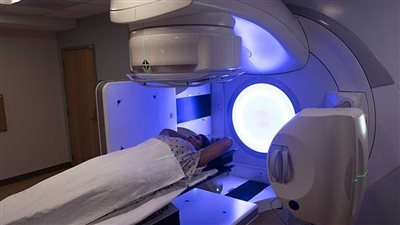
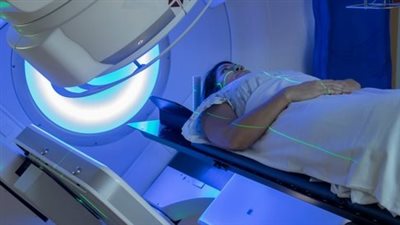
كيف يمكن التغلب على مقاومة الورم للعلاج الإشعاعي؟
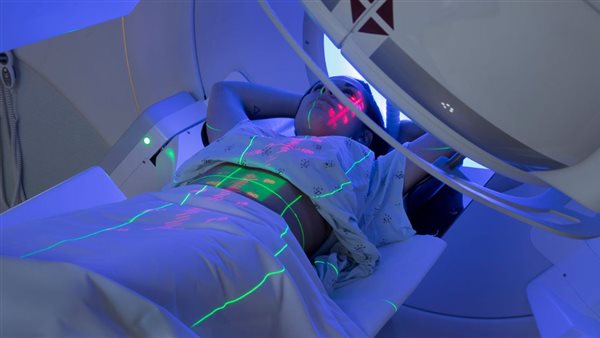
كشف فريق بحثي عن آلية حاسمة تساعد في تنظيم إصلاح تلف الحمض النووي، مع آثار مهمة لتحسين نتائج علاج السرطان.
نُشرت النتيجة في مجلة Cell Death & Differentiation.
قاد الفريق البروفيسور تشاو جوبينج من معاهد هيفاي للعلوم الفيزيائية التابعة للأكاديمية الصينية للعلوم.
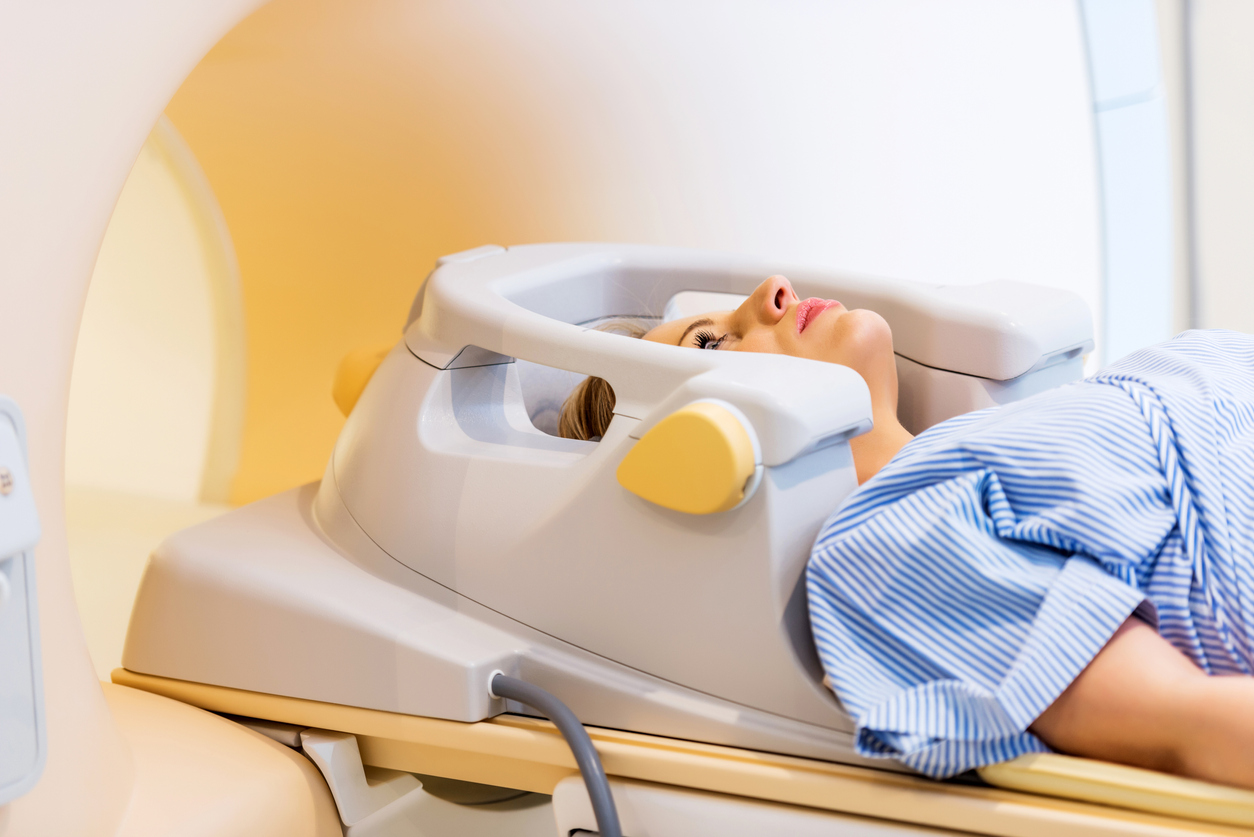
فعالية العلاج الإشعاعي
فعالية العلاج الإشعاعي محدودة إلى حد كبير بقدرة الخلايا السرطانية على إصلاح تلف الحمض النووي.
عندما يُسبب الإشعاع المؤين تكسرًا مزدوجًا في سلسلة الحمض النووي - وهو الضرر المميت الأساسي - غالبًا ما تُظهر الخلايا السرطانية فرطًا غير طبيعي في التعبير عن بروتينات إصلاح الحمض النووي، مما يُنشئ نظام استجابة قويًا للتلف يُحفز مقاومة الإشعاع السريرية.
ولمواجهة هذا التحدي، فكّ الفريق شفرة الشبكة التنظيمية للتعديلات فوق الجينية في إصلاح تلف الحمض النووي.
وجدت الدراسة أن بروتين إصبع الزنك ZNF451 يُعبَّر عنه بشكل مفرط في سرطان الثدي وسرطان الرئة وأورام خبيثة أخرى، مما يرتبط بسوء تشخيص المريض.
أظهرت الدراسات الميكانيكية أنه عند تلف الحمض النووي الناتج عن الإشعاع، يتراكم ZNF451 بسرعة في مواقع التلف، ويحفز تحديدًا تعديل SUMO 2 لـ RNF168.
يُثبِّت هذا التعديل ما بعد الترجمة RNF168، مما يُعزِّز تجنيده لمواقع التلف، مما يُضخِّم اليوبيكويتين اللاحق للهيستون H2A/H2AX، ويعزز في النهاية إصلاح الحمض النووي.
كشف الفريق أيضًا عن شبكة تنظيمية ديناميكية بين ZNF451 وعامل الإصلاح الأساسي RNF8.
يُعدّل هذان البروتينان نشاط RNF168 من خلال الارتباط التنافسي والتفاعلات التعاونية.
وبشكل أكثر تحديدًا، يُثبّط كلٌّ من ZNF451 وRNF8 استقطاب RNF168 من الآخر، إلا أن النضوب المتزامن لكليهما يُضعف بشدة تراكم RNF168 في مواقع التلف.
وقد أظهر التحليل الكمي أن ZNF451 وRNF8 يُحسّنان قوة التفاعل بين RNF168 وركائزه H2AX، اعتمادًا على الجرعة.
لا تسلط هذه الدراسة الضوء على آلية جديدة تنظم من خلالها عملية SUMOylation إصلاح تلف الحمض النووي فحسب، بل تقترح أيضًا نموذجًا مبتكرًا "لتنظيم التوازن الديناميكي"، مما يوفر تقدمًا نظريًا في فهم آليات إصلاح الحمض النووي.