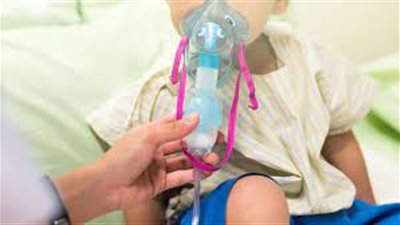
أمل جديد لمكافحة الفيروس المخلوي التنفسي (RSV).. ماذا حدث؟
في كل عام في أشهر الشتاء، هناك موجات من العدوى بـ الفيروس المخلوي التنفسي (RSV)، وفي البالغين والمراهقين الأصحاء، عادة ما تكون العدوى غير ضارة، لكن الأمر ليس كذلك بالنسبة للأطفال الصغار.
فحوالي 1% منهم الذين يتعرضون لمسببات المرض لأول مرة يصابون بمرض خطير للغاية بحيث يتعين عليهم دخول المستشفى.
كما يمكن أن يسبب مرضًا خطيرًا لدى البالغين الذين تزيد أعمارهم عن 65 عامًا بسبب أمراض القلب أو الرئة الموجودة مسبقًا.
تمت الموافقة على اللقاحات لكبار السن والنساء الحوامل منذ عام 2023، ولكن لا يوجد حاليًا علاج مباشر مضاد للفيروسات ضد فيروس الفيروس المخلوي التنفسي (RSV).
من أجل اكتشاف مواد فعالة جديدة ضد مسببات أمراض معينة، يبحث الباحثون في مجموعات كبيرة من المواد المعروفة بالفعل والتي تم اختبارها سريريًا.
تُعرف هذه العملية باسم «شاشة إعادة استخدام الأدوية» وتفحص مجالات التطبيق الإضافية للمستحضرات الصيدلانية المعروفة بالفعل.
استخدم فريق من معهد علم الفيروسات التجريبي في TWINCORE، مركز أبحاث العدوى التجريبية والسريرية، في هانوفر، بقيادة توماس بيتشمان، هذه الطريقة للبحث في مكتبة ReFRAME التابعة لمعهد سكريبس للأبحاث (الولايات المتحدة) عن أدوية الفيروس المخلوي التنفسي (RSV) الجديدة المحتملة.
يحتوي بنك المواد هذا على حوالي 12 ألف مادة فعالة قيد التطوير السريري أو تمت الموافقة عليها بالفعل.
يقول بيتشمان: «لفحص المكتبة، استخدمنا ما يسمى بفيروس المراسل الذي يحمل بروتين الفلورسنت GFP، يشير عدم وجود رد فعل مضان في هذا الاختبار إلى وجود تأثير مضاد للفيروسات».
وفي الوقت نفسه، تم أيضًا تحليل سمية جميع المواد.
يتم إدراج فقط تلك التي ليس لها تأثير مدمر للخلايا في القائمة المختصرة.
تم إجراء الاختبارات تلقائيًا باستخدام روبوت السحب بالتعاون مع معهد علم الفيروسات في كلية الطب في هانوفر.
وقالت سيبيل هايد، العالمة في معهد علم الفيروسات التجريبية والمؤلفة المشاركة للدراسة: «خلافًا لذلك، يكاد يكون من المستحيل التدقيق في مجموعة مكونة من عدة آلاف من المواد».
ومن بين 21 مرشحًا متبقيًا، ركز العلماء على المادة الفعالة lonafarnib، والتي تمت الموافقة عليها لعلاج متلازمة هاتشينسون-جيلفورد بروجيريا.
الأشخاص المصابون بهذا المرض الوراثي النادر يتقدمون في السن مبكرًا ويموتون مبكرًا، في المتوسط، عند عمر 14.5 عامًا.
وقالت هايد: «يمنع لونافارنيب خطوة نضج محددة للبروتينات في الخلية».
ومن أجل توصيف آلية العمل ضد فيروس RS بشكل أكثر دقة، اختبر الباحثون مثبطًا آخر للفارنيسيليشن يسمى تيبيفارنيب وقارنوا النتائج.
وأأوضحت هايد: «لا يعمل تيبيفارنيب ضد الفيروس المخلوي التنفسي، ومن هذا، تمكنا من استنتاج أن التأثير المضاد للفيروسات للونافارنيب ربما لا يعتمد على تثبيط فارنيسيليشن».
وبمساعدة شركاء التعاون آنا هيرش من معهد هيلمهولتز للأبحاث الصيدلانية سارلاند (HIPS) وتوماس كري من جامعة لوبيك، تمكن الفريق من توضيح التركيب الجزيئي لمجمع الدواء والفيروس. يرتبط Lonafarnib ببروتين الاندماج في الفيروس المخلوي التنفسي (RSV) وبالتالي يمنع الفيروس من الاندماج مع غشاء الخلية المستهدفة، ونتيجة لذلك، لا يمكن إصابة أي خلايا جديدة.
وبالتعاون مع زملاء في فرنسا، تم بالفعل إثبات انخفاض في الحمل الفيروسي في نموذج الفأر.
يقول بيتشمان: «ومع ذلك، فإن جرعة لونافارنيب المطلوبة لتناوله عن طريق الفم عالية جدًا، لذلك لاحظنا أيضًا آثارًا جانبية، من المتصور أن التطبيق الموضعي، على سبيل المثال، عن طريق الاستنشاق، يمكن أن يحسن النسبة بين التأثير والأثر الجانبي، ويجب فحص ذلك بعناية في دراسات المتابعة».
وقالت سفينيا ساكي، المؤلفة الأولى للدراسة: «مع لونافارنيب، حددنا مرشحًا مثيرًا للاهتمام لعلاج الفيروس المخلوي التنفسي».
وأضافت: «نظرًا لأن الدواء قد خضع بالفعل لجميع التجارب السريرية، فإن الموافقة على المؤشر الجديد ستكون أسهل بكثير، وأرخص، وأسرع من الموافقة على مادة نشطة جديدة تمامًا».
وقال قائد الدراسة بيتشمان: «تعد هذه الدراسة أيضًا مثالًا رائعًا آخر على العمل الجماعي، كما هو معتاد في العلوم، نحن نتواصل مع العديد من شركاء التعاون في مجموعة RESIST للتميز، على سبيل المثال».