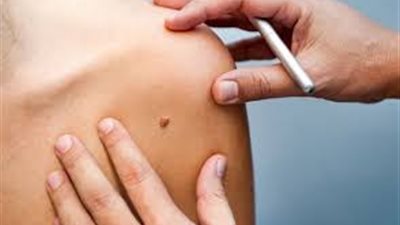
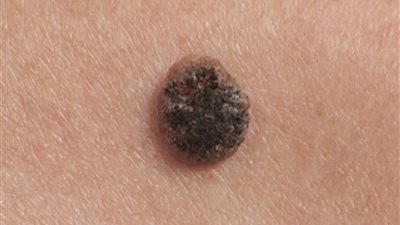
سمة وراثية تتنبأ بمقاومة العلاج المناعي لسرطان الجلد القاتل
كشفت اختبارات أُجريت على 1225 مريضا مصابا بأخطر أنواع سرطان الجلد، لأول مرة، عن سمة وراثية لدى معظم من لم يستجيبوا لأحدث علاجات السرطان، والمعروفة باسم مثبطات نقاط التفتيش المناعية.
يقتل الورم الميلانيني النقيلي، كما يُسمى رسميًا، ما يقرب من 10 آلاف أمريكي سنويًا.
في حين أثبتت الأدوية نجاحها الكبير في علاج الورم الميلانيني النقيلي والعديد من أنواع السرطان الأخرى، فمن المعروف أن هذه العلاجات لا تعمل مع ما يقرب من نصف أولئك الذين يصف لهم الطبيب هذه الأدوية، وعادة ما يكون ذلك بعد فشل العلاج الكيميائي الأولي أو الجراحة في وقف نمو الخلايا السرطانية الجديدة.
وتضمنت الدراسة الجديدة، التي أجراها باحثون في مركز NYU Langone Health ومركز Perlmutter Cancer Center التابع له، تحليلاً جينياً لعينات الدم من تجربة CheckMate-067 المرحلة الثالثة المستمرة والتي تُجرى في أكثر من 100 مركز طبي في 19 دولة.
وأظهرت نتائج الدراسة أن المرضى الذين لديهم نوع معين من الطفرات الجينية، يسمى MT haplogroup T (HG-T)، كانوا أقل احتمالا بنحو 3.46 مرة للاستجابة لعلاج نقطة التفتيش من أولئك الذين لا يعانون من HG-T.
الطفرات هي تغيرات مُشفَّرة في الحمض النووي لخلايا شاذة أو مختلفة.
وقد وجد الباحثون تغيرات HG-T في الميتوكوندريا، وهي هياكل خلايا قوية، لدى مرضى مقاومين للعلاج المناعي.
يتميز الحمض النووي للميتوكوندريا بأنه ينتقل من الأم إلى أبنائها فقط، دون أي مساهمة جينية أو نسخة من الأب، كما هو الحال عادةً في مركز التحكم في الخلية، أو الحمض النووي النووي.
مع مرور الوقت، تطور الحمض النووي للميتوكوندريا عالميًا إلى مجموعات فرعية مُصنفة من الألف إلى الياء بناءً على طفراتها المشتركة.
ونشر الباحثون في مجلة "نيتشر ميديسن" أنهم قرروا التركيز على الحمض النووي للميتوكوندريا ليس فقط بسبب نسبه الفريد ولكن أيضًا بسبب الأبحاث السابقة التي أظهرت أنه لعب دورًا في تطور الخلايا المناعية.
في تجربة "تشيكميت"، استُخدمت أدوية العلاج المناعي، مثل نيفولوماب، بمفردها أو بالاشتراك مع مثبط آخر لنقاط التفتيش، وهو إيبيليموماب، لمنع عودة الورم الميلانيني بعد الجراحة.
تعمل هذه الأدوية عن طريق حجب الجزيئات (نقاط التفتيش) الموجودة على سطح الخلايا التائية المناعية لمنعها من مهاجمة الخلايا السرطانية كما تفعل مع الفيروسات أو البكتيريا الغازية.
يستخدم الجسم عادةً نقاط التفتيش للتعرف على الخلايا السليمة، ولكن في السرطان، تستغل خلايا الورم هذه النقاط وتُعطلها للتهرب من اكتشاف الجهاز المناعي.
تعوق العلاجات المناعية هذه النقاط، مما يجعل خلايا السرطان أكثر وضوحًا وعرضةً للخلايا المناعية.
للتحقق من صحة نتائج "تشيكميت"، راجع الباحثون نتائجهم الأولية مع عينات من 397 مريضًا بسرطان الجلد النقيلي من نفس العمر والجنس، والذين حُفظت سجلات علاجهم المناعي في مركز لانجون بجامعة نيويورك كجزء من الاتحاد الدولي لعلم الأورام المناعية للخلايا الجرثومية (IO-GEM)، وكشفت النتائج مجددًا عن نفس الصلة بين مقاومة العلاج المناعي وHG-T.
قال الباحث المشارك في الدراسة وخبيرة علم الأوبئة الدكتورة كيسلي مونسون: "أصبح العلاج المناعي عند نقاط التفتيش الركيزة الأساسية في علاج السرطان في العقد الماضي، وخاصة بالنسبة لأولئك الذين يعانون من الورم الميلانيني النقيلي، ولكن حتى الآن لم يتم تفسير سبب عدم استجابة ما يقرب من نصف هؤلاء للعلاج بشكل واضح".
وقال الباحث المشارك في الدراسة وعالم الأحياء الجزيئية الدكتور روبرت فيرجسون: "تقدم نتائج دراستنا أول دليل علمي على وجود علامة بيولوجية وراثية، أو وجود طفرة في الميتوكوندريا تعرف باسم المجموعة الفرعية MT T، للمساعدة في تفسير وتحديد مرضى الورم الميلانيني النقيلي الذين من المرجح ألا يستجيبوا للعلاج المناعي للمرض".
من بين النتائج الرئيسية الأخرى للدراسة أن مرضى HG-T المقاومين للعلاج لديهم خلايا تائية أقل نموًا مقارنةً بالمرضى غير المقاومين الذين لا يملكون HG-T.
وقد عزا الباحثون هذا التمايز الضعيف إلى زيادة مقاومة أنواع الأكسجين التفاعلية (ROS)، وهي مواد كيميائية مرتبطة عادةً بالالتهاب، مما يشير إلى أن HG-T يوفر نوعًا من الحماية التي توفرها أنواع الأكسجين التفاعلية، مما يعوق هجوم الخلايا التائية.